Leia outros artigos :
 |
| Gripe: Comparação dos fatores do hospedeiro identificados |
Ferramenta de triagem genética identifica como o vírus da gripe (influenza) se infiltra nas células
Pesquisadores da Universidade de Chicago desenvolveram uma ferramenta de triagem genética que identificou dois fatores-chave que permitem que o vírus influenza infecte células pulmonares humanas. A técnica usa novas ferramentas de edição de genes para criar uma biblioteca de células modificadas, cada qual com um gene diferente, permitindo aos cientistas ver quais mudanças afetam sua resposta à gripe. Isto, por sua vez, poderia identificar alvos potenciais para drogas antivirais.
"Nossos tratamentos atuais para a gripe são limitados. As vacinas têm eficácia variável, e o vírus tem uma propensão a sofrer mutações para que os medicamentos antivirais não funcionem tão bem", disse Julianna Han, estudante de microbiologia da Universidade de Chicago e principal autora do estudo. publicado em 10 de abril de 2018 em Cell Reports . "A próxima onda de tratamentos antivirais será em parte direcionada ao hospedeiro, então nosso trabalho nos ajuda a entender melhor quais proteínas e vias são utilizadas pelo vírus da gripe".
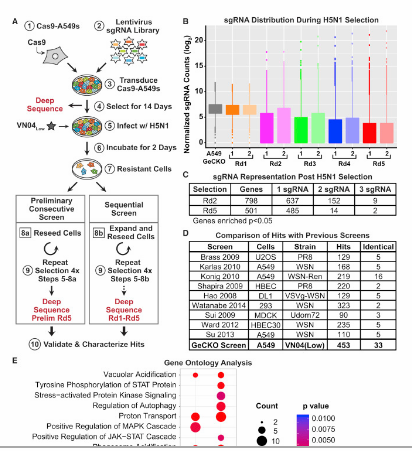
Foram usadas ferramentas de edição do gene CRISPR / Cas9 que permitem aos cientistas eliminar seletivamente, ou desligar genes específicos. Eles criaram uma biblioteca de células pulmonares epiteliais humanas modificadas, as células que revestem as vias aéreas que são as primeiras a serem infectadas pelo vírus da gripe. Cada célula estava faltando um gene diferente, criando cerca de 19.000 variações genéticas diferentes da célula.
Os pesquisadores então expuseram as células à cepa H5N1, um tipo de vírus influenza A conhecido comumente como a gripe aviária. Se o vírus foi capaz de infectar e matar uma das células hospedeiras, isso significa que o gene e as proteínas tiveram um papel na capacidade do vírus de se replicar. Se a célula sobreviveu, isso significa que seu genoma modificado de alguma forma a tornou resistente ao vírus - agora estava faltando um caminho em que o vírus dependia para replicar e fazer seu trabalho sujo.
Após cinco rodadas de exposição das células ao vírus H5N1, Han e Manicassamy ficaram com um conjunto de células que eram bastante resistentes à gripe.
O gene CIC, é mais intrigante. É um regulador negativo do sistema imunológico inato, o que significa que ajuda a desligar a resposta imune padrão da célula a invasores estrangeiros. Quando o CIC é desligado, outros genes que produzem respostas antivirais e inflamatórias são liberados e combatem o vírus, razão pela qual as células de teste que o faltam são resistentes à gripe.
Mas você não pode simplesmente eliminar um gene como o CIC permanentemente como meio de combater a gripe. O corpo precisa de mecanismos para desligar o sistema imunológico uma vez que a infecção desapareça para não danificar as próprias células do corpo, que é o que acontece em distúrbios auto-imunes. Por outro lado, certos tipos de câncer podem explorar um regulador negativo como o CIC para suprimir as respostas imunes, enquanto as células do tumor correm desenfreadamente.
"Ao desligar o CIC, agora permitimos a expressão de genes antivirais capazes de responder à infecção da gripe", disse Manicassamy.
Uma vez que eles identificaram os dois genes-chave envolvidos na resposta ao H5N1, Han e Manicassamy expuseram as células a outros patógenos para identificar mais pontos em comum. O CIC também era importante para todas as cepas de gripe e vários vírus de RNA, ou vírus contendo genomas de RNA. Estes incluíram vírus respiratórios e não respiratórios, destacando o amplo efeito dos CICs.
O novo processo de triagem genética poderia ser usado para encontrar outros genes hospedeiros relevantes para diferentes vírus que infectam células pulmonares epiteliais. Então, os pesquisadores poderiam procurar por qualquer droga atualmente disponível que vise esses caminhos e ver se eles podem ser reaproveitados como tratamentos antivirais.
Em última análise, Han está trabalhando para entender exatamente como o CIC regula outros genes antivirais e inflamatórios.
"É através de mutações no próprio CIC ou através de uma regulamentação aberrante", disse ela. "Se pudermos identificar ainda mais o que está envolvido, podemos tentar descobrir como o CIC está sendo mal regulado em câncer e doenças auto-imunes."
Editado e traduzido
É obrigatório o link da postagem :Ferramenta de triagem genética identifica como o vírus da gripe (influenza) se infiltra nas células
Fonte:http://www.cell.com/cell-reports/fulltext/S2211-1247(18)30387-5